Uso di una miscela di estratti altamente standardizzati di Vitis vinifera, Ginkgo biloba di Melilotus officinalis nel trattamento della cellulite: un approccio biofarmaceutico


Con il termine “cellulite” è stata descritta per la prima volta tra il 1850 e il 1920 un’alterazione estetica evidentemente manifesta sulla parte più superficiale cute, questo non è del tutto corretto in quanto in letteratura scientifica la “cellulite” indicherebbe una diffusione infettiva al tessuto cellulare sottocutaneo. Per questo nel tentativo di fornire una più corretta definizione nel tempo, sono stati usati da diversi autori molti termini più descrittivi, tra cui: pannicolite, lipodistrofia, pannicolite edematofibrosclerotica, liposclerosi, lipoedema, adiposi edematosa, dermopanniculosi deformante, stato protrusus cutis, lipodistrofia ginecologica (GLD), liposclerosi nodulare, pannicolopatia fibrosclerotica edematosa e pannicolosi; creando nel complesso una notevole confusione. Al di là delle definizioni ben poco risolutive, si stima che questa patologia interessi in qualche misura tra l’85 e il 98% della popolazione femminine, fattore per cui alcuni autori hanno finito con il considerarla al pari di una caratteristica sessuale secondaria. La sua insorgenza vede degli aspetti fisiopatologici molto complessi, che includono l’espansione di il tessuto adiposo sottocutaneo, la formazione di setti fibrotici di tessuto connettivo che collegano il piano muscolare al derma compartimentano gli adipociti in una sorta di “camere”. Nel tempo questo conduce a modificazione ed atrofia di numerose componenti dermiche esitando nel tempo in una progressiva lassità cutanea. Questi processi possono includere un ulteriore incremento di peso sia dovuto alla componente adiposa sia all’incremento nella ritenzione di fluidi, manifestandosi con il caratteristico aspetto a “buccia d’arancia”, con particolare salienza a livello dell’area glutea, trocanterica, pelvica e addominale. La somma di questi effetti sembra correlata secondo alcuni autori all’insufficienza degli sfinteri precapillari interessati dallo sviluppo della cellulite, dati da flussimetria laser doppler mostrano una riduzione media del flusso del 35% nelle regioni colpite rispetto alle regioni non colpite. Inoltre, in favore di questa ipotesi dati riportati in studi datati ma interessanti riportano variazioni nel contenuto proteico e incremento della pressione interstiziale. Sembra che alla base di questo quadro possano esserci fattori genetici ed esposomici:
Fattori genetici:
- Sesso: il sesso femminile sembra essere quello prevalentemente interessato dalla manifestazione in forma classica.
- Etnia: l’origine caucasica è correlata a una maggiore tendenza nella manifestazione rispetto all’asiatica, africana o afroamericana.
- Biotipo: in genere sembra che le donne latine sviluppino maggiori manifestazioni a livello dei fianchi mentre quelle anglosassoni e nordiche sviluppino maggiori manifestazioni a livello addominale
- Distribuzione del tessuto adiposo
- Numero, isoforma e sensibilità dei recettori ormonali sulle cellule interessate
- Predisposizione a sviluppo periferico di angiopatia (o suscettibilità allo sviluppo di insufficienza circolatoria)
Fattori esposomici:
- Dieta squilibrata (in genere eccessivo apporto di grassi e carboidrati);
- Eccessivo apporto di sodio (ritenzione di liquidi);
- Dieta povera di fibre (costipazione con relativo aumento della resistenza venosa)
- Stile di vita sedentario (con diminuzione di massa muscolare, aumento della massa grassa, aumento della flaccidità di tendini e muscoli, diminuzione del meccanismo di “pompa muscolare” la somma di questi effetti favorisce l’incremento della stasi circolatoria).
La progressione di un quadro di cellulite può essere classificata in diverse maniere, tra le diverse proposte quella di Rossi e Vergagnini, pur con diversi limiti costituisce una delle metodiche di più rapida e semplice attuazione ambulatoriale:
Grado I: il paziente è asintomatico e non ci sono alterazioni cliniche.
Grado II: Non si evidenziano cambiamenti a riposo, ma dopo la compressione della cute o dopo contrazione muscolare si evidenzia pallore, diminuzione della temperatura e diminuzione dell’elasticità. Non ci sono alterazioni del sollievo a riposo ma
Grado III: È evidente anche a riposo un aspetto della cute “imbottito” o a “buccia di arancia”, sono palpabili sottili granulazioni sui piani più profondi del derma, si evidenziano alla palpazione dolorabilità, ridotta elasticità, pallore e diminuzione della temperatura.
Grado IV: Si manifesta in maniera analoga al grado III ma con una maggiore salienza dei reperti riscontrabili sia visivamente sia alla palpazione, con pronunciata aderenze nei livelli più profondi del derma e un evidente aspetto “ondulato” riscontrabile a livello superficiale.
Con l’obiettivo di fornire un supporto alla terapia della cellulite un recente studio pubblicato su Nutrafoods ha preso in considerazione gli effetti riscontrabili con la somministrazione di estratti altamente standardizzati e biodisponibili di Vitis vinifera, Ginkgo biloba e Melilotus officinalis sui parametri antropometrici legati alla cellulite, e di conseguenza, sul decorso della patologia
Panoramica dello studio
Lo studio è stato effettuato in maniera retrospettiva su soggetti che volontariamente hanno seguito un cambiamento strutturato e uniforma dello stile di vita finalizzato al trattamento della cellulite che includesse l’assunzione per 90 giorni di due diversi integratori; una miscela di estratti altamente standardizzati e biodisponibili di Vitis vinifera, Ginkgo biloba e Melilotus officinalis al dosaggio di 2 o 3 compresse giorno e l’assunzione di una preparazione galenica a base di carnosina e beta alanina. I gruppi che assumevano gli estratti sono stati valutati come gruppi di “trattamento” mentre il gruppo che assumeva la preparazione galenica è stato utilizzato come gruppo controllo. Per ogni soggetto sono stati valutati peso, altezza e le circonferenze di vita, fianchi, coscia prossimale, coscia mediana, coscia distale e polpaccio. I dati ottenuti nei diversi gruppi sono stati elaborati con il test t di Student per la verifica dell’ipotesi su valori medi. Il lavoro è stato svolto in conformità con le “buone pratiche cliniche” stabilite dalla Dichiarazione del Helsinki in conformità con la Direttiva dell’Unione Europea 2001/20 / CE. Ogni paziente ha firmato un modulo di consenso informato e relativo al trattamento e analisi dei dati
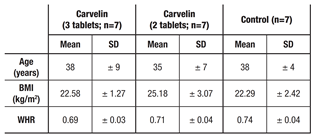
Sono stati presi in considerazione dati relativi a 21 donne adulte di età compresa tra 24 e 53 anni che si sono volontariamente sottoposte a un programma di cambiamento dello stile di vita per il trattamento della cellulite che include attività motoria. Sono stati presi in considerazione soggetti in normopeso e sovrappeso (BMI compreso tra 19 e 29,7 kg / m2), con accumulo adiposo di carattere ginoide secondo il metodo proposto da Björntorp, anche se come riportato in letteratura questi parametri non sono decisivi per lo sviluppo e progressione della cellulite. Tutti i 21 soggetti sono stati valutati secondo il metodo proposto di Rossi e Vergnanini, 17 erano classificabili come grado II e 4 come grado III. Soggetti di grado I e IV non sono stati inclusi in quanto caratterizzati da condizioni troppo diverse rispetto agli altri soggetti valutati. Sono state escluse dallo studio le donne che non avevano presenza di attività mestruale, in gravidanza, in trattamento con estro-progestinici, anticoagulanti, antinfiammatori, flebotropi, con patologie in atto, che stavano contestualmente eseguendo altri trattamenti per specifici per la cellulite, che avevano inserito altri cambiamenti non richiesti nello stile di vita (fumodi sigaretta, consumo di alcool ecc), che hanno iniziato il programma di attività motoria da più di 3 giorni dall’inizio della raccolta dei dati o che svolgevano anche ulteriore attività fisica oltre a quella programmata (2 sedute di attività aerobica della durata di 45 minuti eseguite settimanalmente).
In totale sono stati valutati 21 soggetti di cui 7 hanno assunto 2 compresse / giorno e 7 hanno assunto 3 compresse / giorno di una miscela di estratti di Vitis vinifera, Ginkgo biloba e Melilotus officinalis formulato in compresse a 3 strati, prodotto da SIIT (Trezzano sul Naviglio, Milano, Italia) e notificato al Ministero della Salute italiano come un integratore alimentare di Pharmextracta SpA (Pontenure, PC, Italia) in ottemperanza alla legge n ° 196- 2004 (numero di notifica: 22435), commercializzato sotto il nome di “Carvelin”. Le compresse contenevano nello strato superiore (a rilascio di 30/45 minuti) 100 mg di Leucoselect Phytosome® (da Vitis vinifera), nello strato centrale (8 ore rilascio prolungato) 50 mg di Lymphaselect® (da Melilotus officinalis) e nello strato inferiore (Rilascio 30/45 minuti) 80 mg di Ginkgoselect Phytosome® (da Ginkgo biloba). Leucoselect Phytosome® corrisponde a una miscela altamente standardizzata di oligomeri procianidolici (OPC – proantocianidine: 25,0-30,0%), estratte dalla parte esterna di semi di Vitis vinifera, complessati con distearoilfosfatidilcolina di soia (Glycine max). Lymphaselect® corrisponde a un estratto altamente standardizzato da parti aeree di Melilotus officinalis titolato a resa ≤20% cumarine. Ginkgoselect Phytosome® corrisponde a un estratto altamente standardizzato di foglie di Ginkgo biloba (ginkgoflavonglicosidi ≥7,0%, ginkgoterpeni ≥2,0%, bilobalide ≥0,8%, ginkgolidi ≥0,8%, acidi ginkgolici totali ≤5 ppm), complessato con distearoilfosfatidilcolina di soia (Glycine max). Carvelin è stato utilizzato con la logica di supportare la circolazione funzione attraverso l’azione sinergica dei suoi componenti. I restanti 7 partecipanti hanno assunto un preparato galenico contenente 250 mg di carnosina e 250 mg di beta-alanina, presi con la logica di supportare la funzione tampone del muscolo scheletrico promuovendo l’esecuzione del programma di attività fisica incluso nel programma di cambiamento dello stile di vita; questo gruppo come accennato è stato usato come controllo.
Risultati
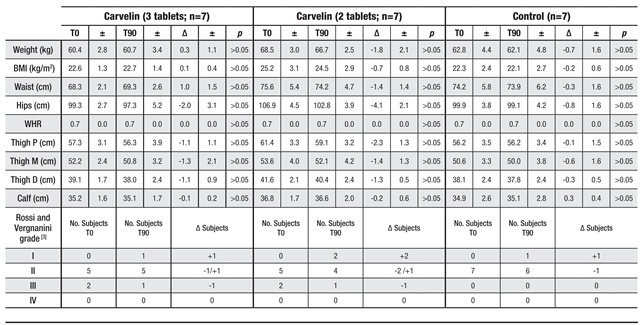
Alla fine del periodo di valutazione, considerando l’entità delle variazioni e la deviazione standard, non erano apprezzabili variazioni di peso, BMI, circonferenza vita o del rapporto vita-fianchi (WHR). La circonferenza dei fianchi si è ridotta di 2 cm ± 3,1 (p> 0,05), 4,1 cm ± 2,1 (p> 0,05) e 0,8 cm ± 1,6 (p> 0,05), rispettivamente, nei gruppi Carvelin 3, Carvelin 2 e di controllo. La valutazione delle circonferenze della coscia ha mostrato rispettivamente le seguenti riduzioni per i gruppi Carvelin 3, Carvelin 2 e controllo: coscia prossimale 1,1 cm ± 1,1 (p> 0,05), 2,3 cm ± 1,3 (p> 0,05), 0,1 cm ± 1,5 (p> 0,05); metà coscia 1,3 cm ± 2,1 (p> 0,05), 1,4 cm ± 1,3 (p> 0,05), 0,6 cm ± 1,6 (p> 0,05); coscia distale 1,1 cm ± 0,9 (p> 0,05), 1,3 cm ± 0,5 (p> 0,05), 0,3 cm ± 0,5 (p> 0,05). A livello del polpaccio, non sono state evidenziate differenze significative.
La scala di Rossi e Vergnanini (basata come descritto su valutazioni cliniche e sintomatiche) non prevede la possibilità di punteggi intermedi, rendendo la valutazione delle medie e delle deviazioni standard non propriamente applicabili. Al T0 nel gruppo Carvelin 3 erano presenti 5 soggetti classificati come grado II e 2 come grado III; a T90 1 soggetto originariamente classificato di grado II è stato riclassificato di grado I e 1 soggetto è stato riclassificato dal grado III al grado II. Allo stesso modo, nel gruppo Carvelin 2, a T0 erano presenti 5 soggetti classificati come grado II e 2 come grado III; a T90 2 soggetti originariamente classificati di II grado sono stati riclassificati di grado I e 1 soggetto è stato riclassificati dal grado III al grado II. Nel gruppo di controllo, a T0 erano presenti 7 soggetti classificati come grado II; da T90 1 soggetto originariamente classificato come grado II è stato riclassificato come grado I. Pertanto, anche nella valutazione secondo la scala Rossi e Vergnanini, il Il gruppo Carvelin 2 ha dimostrato risultati superiori. Tutti i dati sono riassunti nella tabella 2.
Discussione
Alla fine dei 90 giorni, i due i sottogruppi che hanno assunto Carvelin hanno mostrato una maggiore riduzione delle circonferenze dei fianchi e della coscia rispetto al gruppo che ha preso il prodotto di controllo, sebbene molte di queste variazioni non fossero statisticamente significative. Il gruppo che ha assunto due compresse al giorno di Carvelin ha mostrato risultati superiori rispetto agli altri 2 gruppi. Effettuando una prima ipotesi di carattere speculativo volta a spiegare i maggiori risultati nel gruppo che ha assunto 2 compresse è possibile considerare il potenziale ruolo dei componenti di Carvelin come induttori dell’attività enzimatica di diversi citocromi. Il Ginkgo biloba ha in vitro un ruolo noto come induttore di CYP2B1 / 2, CYP3A1, CYP3A2 e CYP3A4. La Vitis vinifera è nota per causare in vitro l’induzione del CYP3A4, mentre è noto che il Melilotus officinalis in vitro viene metabolizzato dal CYP2C9. Queste implicazioni metaboliche potrebbero avere un ruolo se considerate per il metabolismo degli estratti vegetali, notoriamente dotati di biodisponibilità piuttosto ridotta rispetto al metabolismo dei farmaci per i quali non sono note interazioni rilevanti clinicamente confermate. Per esempio, nello studio dell’estratto di Ginkgo biloba impiegato in Carvelin, l’ EGb 761® non è stato segnalato in vivo su modello umano nessun effetto rilevante sull’attività dei principali enzimi CYP, non dimostrandosi quindi in grado di causare alterazioni nel metabolismo dei farmaci. Alla luce di questi dati probabilmente l’induzione potrebbe essere ipotizzata esclusivamente nel metabolismo degli estratti vegetali. La ridotta numerosità del campione analizzato e l’esecuzione retrospettiva dello studio possono spiegare, nonostante le riduzioni riscontrate, i risultati del test-t. La futura esecuzione di una valutazione in doppio cieco, randomizzata, placebo-controllato in cui, oltre alla valutazione antropometrica si esegua una valutazione bioimpedenziometrica e ematochimica, potrebbe contribuire in modo significativo a chiarire i risultati ottenuti, spiegando o eventualmente smentendo la maggiore efficacia ottenibile con una dose inferiore.
Conclusioni
Il consumo di una miscela estratti ad alta biodisponibilità, in formulazione biofarmaceutica di Vitis vinifera, Ginkgo biloba e Melilotus officinalis, è correlata a una maggiore riduzione della circonferenza dell’anca e circonferenze della coscia al dosaggio di due compresse / giorno rispetto a tre compresse / giorno e rispetto a un controllo costituito da una preparazione galenica contenente 250 mg di carnosina e 250 mg di beta-alanina. Considerando la ridotta dimensione del campione in studio, i risultati possono essere considerati promettenti; rendendo questo approccio proponibile nella prospettiva di un programma globale per il trattamento della cellulite, fornendo un ulteriore elemento di supporto al trattamento medico, farmacologico, nutrizionale e di attività fisica. Ulteriori studi con un numero maggiore di gli soggetti saranno necessari in futuro per chiarire i risultati ottenuti, indagando quale posologia rappresenta la soluzione più vantaggiosa nel periodo di tempo considerato.
Bertuccioli A, Bressan A, Biagi A, Neri M, Zonzini G. Use of a highly standardized mixture of Vitis vinifera, Ginkgo biloba and Melilotus officinalis extracts in the treatment of cellulite: a biopharmaceutical approach. Nutrafoods (2021) 1:220-226 DOI 10.17470/NF-021-0029
L’articolo originale può essere scaricato al seguente link:
https://www.nutrafoods.eu/wp-content/uploads/2021/01/doi_10.17470_nf-021-0029.pdf